Verantwortliche Person – PRRC (Artikel 15 MDR)
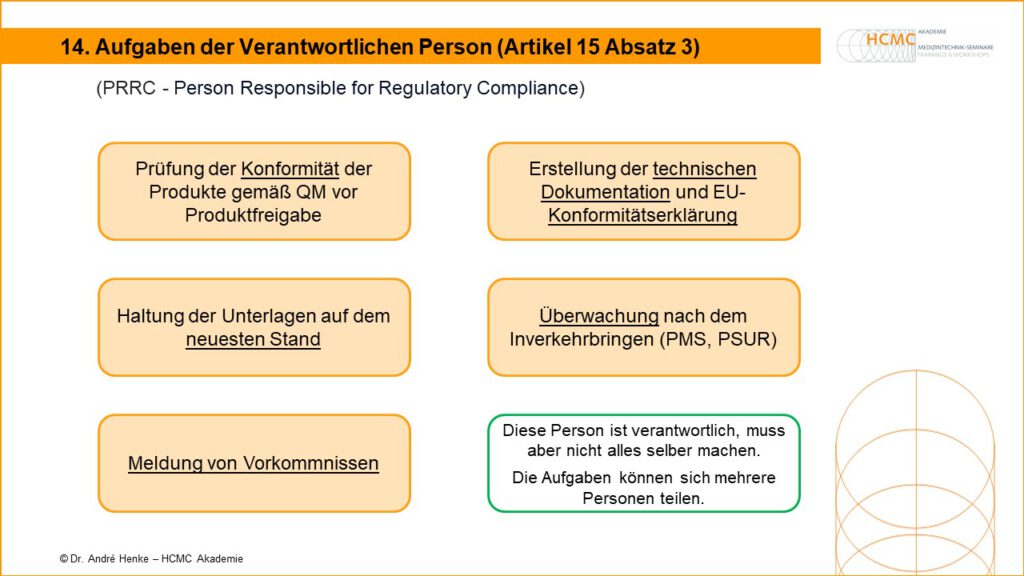
Die verantwortliche Person nach Art. 15 MDR/IVDR ist eine gesetzlich vorgeschriebene Person mit definierten Verantwortlichkeiten, Aufgaben und Anforderungsprofil. Ohne eine verantwortliche Person im Unternehmen (Hersteller) ist eine Zulassung von Medizinprodukten in Europa nicht möglich. Die Aufgaben der Verantwortlichen Person (MDR) sind deutlich umfangreicher als die Aufgaben des Sicherheitsbeauftragten des MPG. Im englischen wird die Verantwortlich Person […]
Anwendungsbereich
Die Festlegung des Anwendungsbereichs ist der erste Schritt der Zulassung eines Medizinproduktes • Der Anwendungsbereich wird durch den Hersteller festgelegt• Maßgeblich für die Einstufung ist die Art der Verwendung Der Anwendungsbereich kann Einfluss auf die Risikoklasse eines Medizinproduktes haben. So können z.B. Katheter mit einer Verweildauer im Körper von weniger als 30 Tagen in der […]
Europäische Medizinproduktegesetze
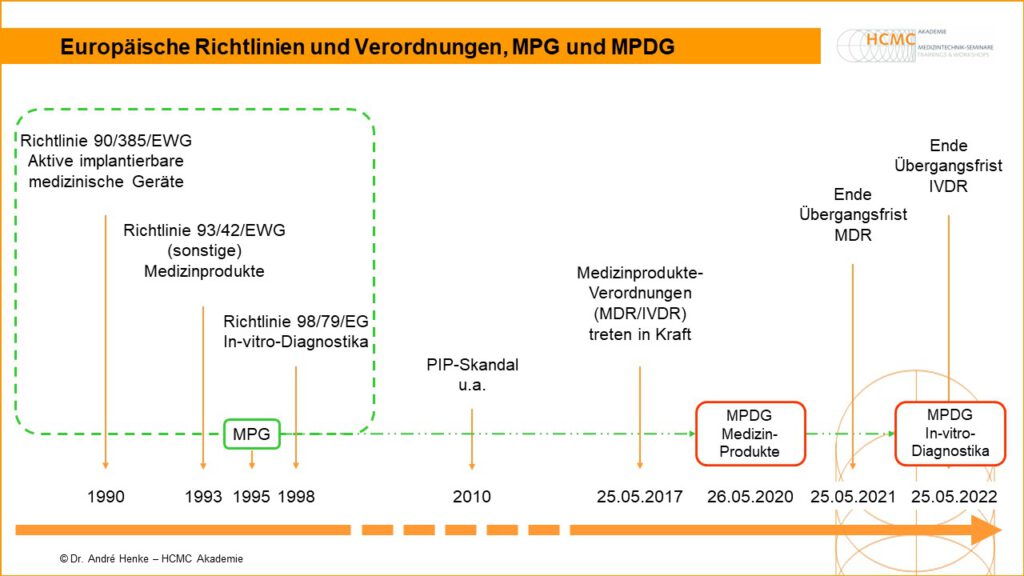
Das Medizinprodukterecht-Durchführungsgesetz (MPDG) dient der Durchführung und Ergänzung der Verordnung (EU) 2017/745. Es ist durch Artikel 1 des Medizinprodukte-EU-Anpassungsgesetzes vom 28. April 2020 (BGBl. I S. 960) eingeführt worden. Das MPDG löst in Deutschland schrittweise ab 26. Mai 2021 das Medizinproduktegesetz für alle Produkte im Anwendungsbereich der Verordnung ab. Es regelt in Ergänzung der europäischen Gesetzte (MDD und MDR) die nationale Umsetzung. […]
Medizinprodukterecht-Durchführungsgesetz MPDG

Das Medizinprodukterecht-Durchführungsgesetz (MPDG) dient der Durchführung und Ergänzung der Verordnung (EU) 2017/745. Es ist durch Artikel 1 des Medizinprodukte-EU-Anpassungsgesetzes vom 28. April 2020 (BGBl. I S. 960) eingeführt worden. Das MPDG löst in Deutschland schrittweise ab 26. Mai 2021 das Medizinproduktegesetz für alle Produkte im Anwendungsbereich der Verordnung ab. Es regelt in Ergänzung der europäischen Gesetzte (MDD und MDR) die nationale Umsetzung. […]
Medizinische Normen

Bei einer Norm handelt es sich um eine anerkannte Regel der Technik, die von Experten im Zuge eines Konsensverfahrens erstellt wird. Damit ist eine Norm eine technische Beschreibung, die für jedermann zugänglich ist und auf abgestimmten Ergebnissen von Wissenschaft, Praxis und Technik beruht. Eine Norm wird von einer anerkannten Organisation gebilligt: Es gibt eine große Anzahl […]
Kombinationsprodukt
Neben den Medizinproduktegesetzen gelten in Deutschland noch weitere Gesetze für medizinische Produkte, wie z.B. das Arzneimittelgesetz. Bei Produkten, die sowohl einen Medizinprodukteanteil, als auch einen Arzneimittelanteil haben, stellt sich die Frage, nach welchem Gesetz das Produkt zuzulassen ist. Beispiel für so ein Produkt ist ein medikamentabgebender Stent für die Herzkranzgefäße. Solche Produkte werden als Kombinationsprodukte […]
Eigenmarke – private labeling
Wenn ein Unternehmen Produkte aus fremder Herstellung (OEM – Produkte) unter seinem eigenen Namen auf den Markt bringt, dann nennt man das Private Labeling bzw. Eigenmarke. Die MDR unterscheidet nicht mehr zwischen Originalherstellern und Eigenmarken. Der „Privat Label Manufacturer – PLM“ ist rechtlich dem Hersteller (Legal Manufacturer) gleichgestellt. Damit muss er alle Verpflichtungen erfüllen. Das […]
Definition Hersteller

„Hersteller“ bezeichnet eine natürliche oder juristische Person, die ein Produkt Der Hersteller lässt die Produkte zu, erstellt die Konformitätserklärung und ist Ansprechpartner für die Behörden. Sollte der Hersteller nicht selbst der Produzent der Produkte sein, sondern „nur“ fremde Produkte unter seinem eigenen Namen vertreiben (Eigenmarke = privat label), so muss er als „PLM – Private […]
Zweckbestimmung

„Zweckbestimmung“ bezeichnet die Verwendung, für die ein Produkt entsprechend den Angaben des Herstellers auf der Kennzeichnung, in der Gebrauchsanweisung oder dem Werbe- oder Verkaufsmaterial bzw. den Werbe- oder Verkaufsangaben und seinen Angaben bei der klinischen Bewertung bestimmt ist. Die Zweckbestimmung wird vom Hersteller festgelegt. Mehr dazu in unseren Seminaren zum Medizinprodukteberater.
Sonderanfertigung

„Sonderanfertigung“bezeichnet ein Produkt, das speziell gemäß einer schriftlichen Verordnung einer aufgrund ihrer beruflichen Qualifikation nach den nationalen Rechtsvorschriften zur Ausstellung von Verordnungen berechtigten Person angefertigt wird, die eigenverantwortlich die genaue Auslegung und die Merkmale des Produkts festlegt, das nur für einen einzigen Patienten bestimmt ist, um ausschließlich dessen individuelle Zustand und dessen individuellen Bedürfnissen zu […]
